درس روائز الكشف عن بعض الأيونات للسنة الثالثة اعدادي في مادة الفيزياء
درس روائز الكشف عن بعض الأيونات في مادة الفيزياء و الكيمياء للسنة الثالثة ثانوي اعدادي و تتضمن فقراته ما يلي :
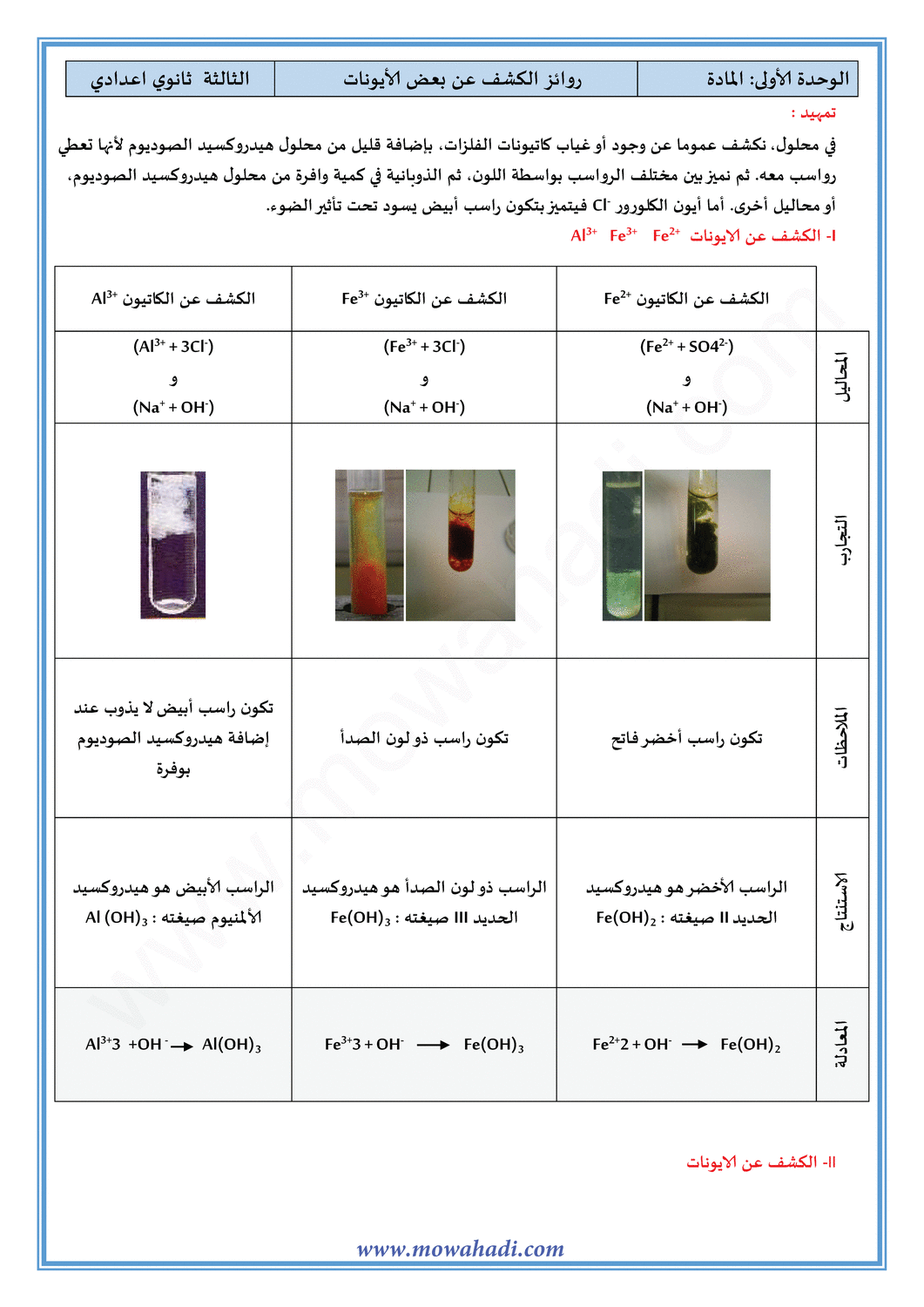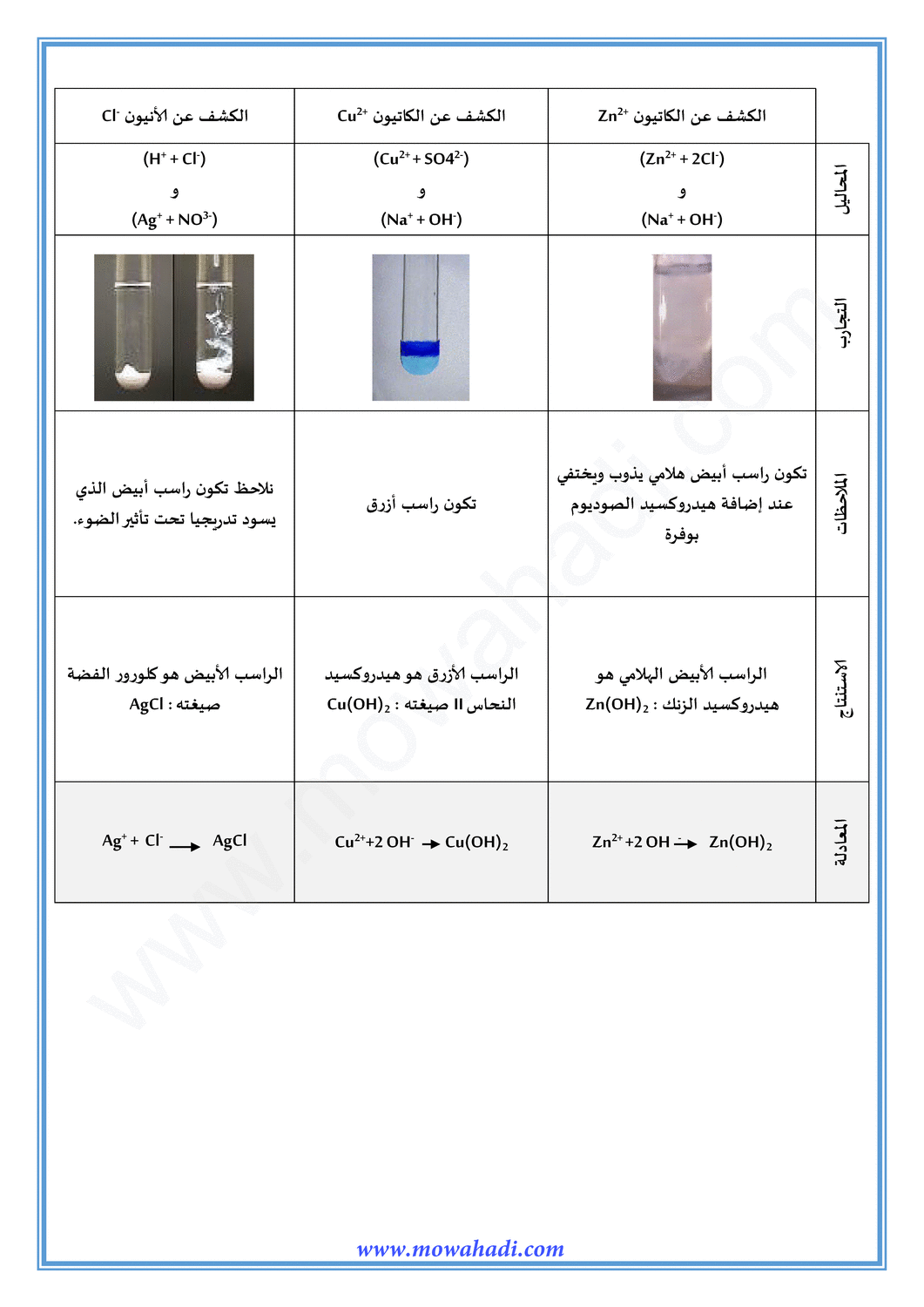
- الكشف عن أيونات الحديد II : فبعد إضافة قطرات من الصودا يتكون راسب أخضر هو هيدروكسيد الحديد II صيغته Fe(OH)2 الذي يدل على وجود أيونات الحديد II Fe2+ في المحلول .
✓ معادلة ترسب هيدروكسيد الحديد II : Fe2+ + 2OH- → Fe(OH)2
- الكشف عن أيونات الحديد III Fe3+ فبعد إضافة قطرات من الصودا يتكون راسب ذو لون بني (لون الصدأ) هو هيدروكسيد الحديد III صيغته Fe(OH)3 ، االذي يدل على وجود أيونات الحديد III Fe3+ في المحلول.
✓ معادلة ترسب هيدروكسيد الحديد III : Fe3+ + 3OH- → Fe(OH)3
- الكشف عن أيونات الألومنيوم Al3+ فبعد إضافة قطرات من الصودا يتكون راسب أبيض لا يذوب في كمية وافرة من محلول هيدروكسيد الصوديوم هو هيدروكسيد الألومنيوم صيغته Al(OH)3 ، االذي يدل على وجود أيونات الألومنيوم Al3+ في المحلول .
✓ معادلة ترسب هيدروكسيد الألومنيوم : Al3++3OH-→ Al(OH)3
الكشف عن أيونات الزنك Zn2+ فبعد إضافة قطرات من الصودا يتكون راسب أبيض هلامي هو هيدروكسيد الزنك صيغته Zn(OH)2 ، االذي يدل على وجود أيونات الزنك Zn2+ في المحلول .
✓ معادلة ترسب هيدروكسيد الزنك : Zn2++2OH- → Zn(OH)2
- الكشف عن أيونات النحاس Cu2+ فبعد إضافة قطرات من الصودا يتكون راسب أزرق هو هيدروكسيد النحاس II صيغته Cu(OH)2 ، االذي يدل على وجود أيونات النحاس Cu2+ في المحلول.
✓ معادلة ترسب هيدروكسيد النحاس II : Cu2++2OH- → Cu(OH)2
- الكشف عن أيونات الكلور Cl- فبعد إضافة محلول نتراث الفضة إلى محلول حمض الكلوريدريك، نلاحظ تكون راسب أبيض يسود تدريجيا تحث تأثير الضوء، يسمى هذا الراسب كلورور الفضة صيغته الكيميائية AgCl ، االذي يدل على وجود أيونات الكلورور Cl- في المحلول.
✓ معادلة ترسب كلورور الفضة : Ag++Cl- → AgCl